Enlace iónico
Un enlace iónico es la unión de átomos que
resulta de la presencia de atracción electrostática entre los iones de distinto
signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y
otro fuertemente electronegativo (alta afinidad electrónica).
Enlace covalente
Un enlace covalente entre dos átomos se
produce cuando estos átomos se unen, para alcanzar el octeto estable,
compartiendo electrones del último nivel (excepto el Hidrógeno que alcanza la
estabilidad cuando tiene 2 electrones).
clasificacion de los elementos
- Metales
- No metales
- La sub clasificaciones
- Grupos
- Periodos
- Familias representativas y sus electrones de valencia
Modelo de Bohr y Lewis
Modelo de Bohr
Niels Bohr se basó en el átomo de hidrógeno para realizar el
modelo que lleva su nombre. Bohr intentaba realizar un modelo atómico capaz de
explicar la estabilidad de la materia y los espectros de emisión y
absorción discretos que se observan en los gases.
Modelo de Lewis
Muestra
el número total de átomos de una molécula, junto con sus respectivos electrones
de valencia, los cuales se representan a través de puntos o rayas. Cabe
mencionar que no se recomienda su uso para estructuras de gran complejidad.
Balanceo de ecuaciones deacuerda a la ley de la conservacion de la masa
informacion
La electronegatividad es una medida de la
capacidad de un átomo (o de manera menos frecuente de un grupo funcional) para
atraer a los electrones, cuando forma un enlace químico en una molécula.
Ejemplos de Electrones
Protones

Neutrones
Un neutrón es una partícula subatómica contenida en el núcleo
atómico refiriéndose que no tiene carga eléctrica, a diferencia de carga
eléctrica positiva del protón.
Subíndice
El subíndice indica el número de moléculas que
se combinan de cada elemento químico, como
en H2.

Coeficientes
Están colocadas después de la flecha o el signo igual a (=).
Los científicos suelen representar las reacciones químicas mediante símbolos y
fórmulas de las sustancias que intervienen y se producen.
Elementos
Un elemento químico es un tipo de materia
constituida por átomos de la misma clase. En su forma más simple posee un
número determinado de protones en su núcleo, haciéndolo pertenecer a una
categoría única clasificada con el número atómico, aun cuando este pueda
desplegar distintas masas atómicas.
Compuestos
Es una sustancia formada por la combinación de dos o más elementos
diferentes de la tabla periódica. Los compuestos son
representados por una fórmula química. Por ejemplo, el agua (H2O)
está constituida por dos átomos de hidrógeno y uno de oxígeno.
Número Atómico
Indica la cantidad de protones que se encuentra presente en el núcleo de un átomo. Este número, por lo tanto, se encarga de definir la configuración electrónica del átomo y permite el ordenamiento de los diversos elementos químicos en la tabla periódica,

Número de masa
El número másico o número de masa es la suma
del número de protones y el número de neutrones del núcleo de un átomo.
Ion
Es una partícula cargada eléctricamente constituida por un átomo
o molécula que no es eléctricamente neutro. Conceptualmente esto se puede
entender como que, a partir de un estado neutro de un átomo o partícula, se han
ganado o perdido electrones; este fenómeno se conoce como ionización.

Anión
Es un ion con carga eléctrica negativa, es decir, que ha
ganado electrones.

Catión
Es un ión con carga eléctrica positiva, es decir, que ha perdido electrones. Los cationes se describen con un estado de oxidación positivo
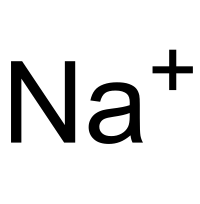
Diferencias entre cambio físico y químico
Si doblamos o arrugamos un papel, cambia de aspecto pero sigue
siendo papel. Decimos que es un cambio físico. Pero si lo quemamos, al
final no queda papel: hay humo y cenizas. Es un cambio químico. Esto
seria un ejemplo




Hey chavales!!! Muy bna informacion xDDDDD lol jaja me hicieron el trabajo de investigacion grax XDDDDD lol jaja
ResponderEliminary los videos
ResponderEliminarEsta pro xDDDDDDDDDDD
ResponderEliminarBuena información me gustan los color:)
ResponderEliminar